آيا mRNA علاوهبر واكسن، در درمان بيماريها نيز متخصصد دارد؟
موفقيت چشمگير دو واكسن كوويد ۱۹ در كارآزماييهاي باليني پيروزي بزرگي براي فناوري پزشكي است كه قبلا اثبات نشده بود. هفتهي گذشته، يكي از اين واكسنها مجوز استفادهي اضطراري را از سازمان غذا و داروي آمريكا دريافت كرد. واكسنهاي مذكور متكيبر دستورالعملهاي ژنتيكي هستند كه با عنوان RNA پيامرسان (mRNA) شناخته ميشود. اين دستورالعملها سلولها را به ساخت يكي از پروتئينهاي SARS-CoV-2 وادار ميكند كه سيستم ايمني را براي شناسايي ويروس يادگيري ميدهد.
مدتها پيش از دنياگيري كوويد ۱۹، mRNA بهعنوان راهي ساده و انعطافپذير براي تحويل واكسن و دارو در انديشه متخصصين گرفته ميشد. توالي خاصي از mRNA ممكن است با توليد پروتئين تحريككنندهي رشد عروق خوني، قلب آسيبديده را ترميم كند. همچنين، توالي ديگر ممكن است آنزيمي را رمزگذاري كند كه بتواند بيماري ژنتيكي نادري را معكوس كند.
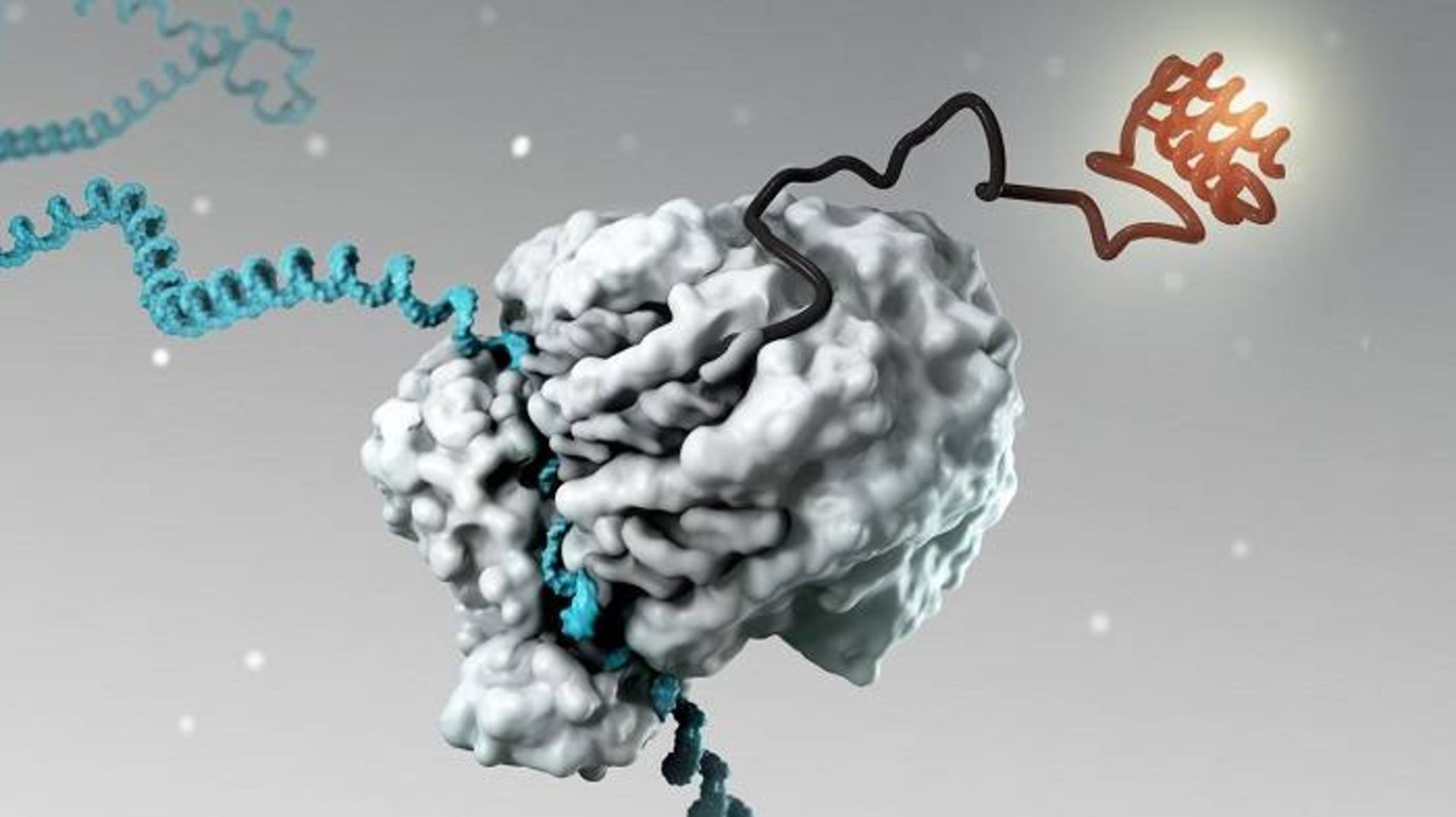
RNA پيامرسان (آبي) ريبواخبار تخصصيهاي سلول را براي ساخت پروتئينهاي جديد (قرمز) هدايت ميكند
گوراو ساهاي، دانشمند داروساز دانشگاه ايالتي اورگن، ميگويد موفقيت واكسنهاي كوويد طوفاني از اشتياق را درزمينهي اين مفهوم ايجاد كرده است. بااينحال، داروهاي mRNA بهويژه داروهايي كه پروتئينهاي مفيد را براي بيماريهاي مزمن جايگزين پروتئينهاي معيوب ميكنند، درمقايسهبا واكسنها مسير سختتري براي رسيدن به كلينيكها پيش رو دارند. اين داروها با چالش هدفگذاري mRNA براي بافتهاي خاص و دادن مزاياي قوي و پايدار بدون عوارض جانبي بيشازحد مواجه هستند.
موارد معدودي از درمانهاي مذكور وارد كارآزماييهاي باليني شدهاند. هلين دويته، دانشمند داروساز دانشگاه گنت بلژيك ميگويد: «اينطور نيست كه توالي ديگري را وارد بدن كنيد و هر چيزي درمان شود.» تطبيق داروي mRNA براي هر بيماري اغلب بهمعناي دستكاري ساختارهاي خود mRNA و حباب محافظي است كه براي انتقال آن به بدن استفاده ميشود و نانوذرهي ليپيدي نام دارد.
براي واكسنها و برخي از داروهاي mRNA استعمال نسبتا ساده است: پس از تزريق در بازو، سلولهاي عضله mRNA را ميگيرند و پروتئين ويروسي را توليد ميكنند و درادامه، سيستم ايمني پروتئين حاصل را بهعنوان عامل خارجي ميبيند و آنتيباديها و سلولهاي T توليد ميكند كه بدن را براي دفاع دربرابر حملهي آينده آماده ميكند. علاوهبر SARS-CoV-2، واكسنهاي mRNA عليه هاري، زيكا، سيتومگالوويروس، آنفلوانزا و ويروسهاي ديگر در كارآزماييهاي باليني در حال پيشرفت هستند.
همچنين، تزريق موضعي به عضله يا زير پوست يا داخل تومور ميتواند درمانهاي مبتنيبر mRNA را به بدن تحويل دهد كه سيستم ايمني را براي مبارزه با سرطان بهكار ميگيرد. چندين كارآزمايي باليني براي چنين درمانهايي در حال انجام است كه پروتئينهاي تومور يا مولكولهاي پيامرسان ايمني را رمزگذاري ميكنند تا به تشديد حمله بدن به سلولهاي سرطاني كمك كند.
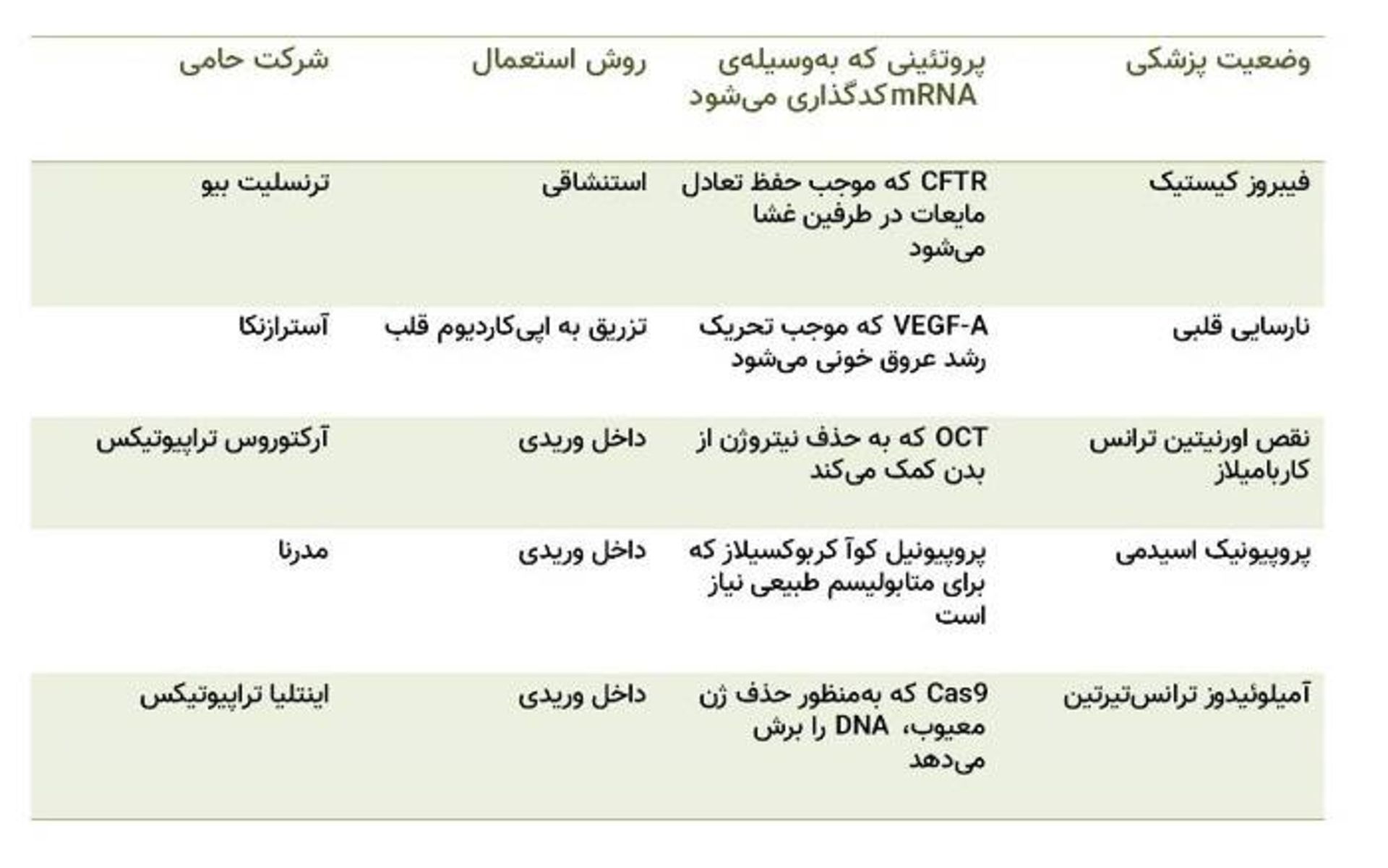
اگرچه كارآزماييهاي متعددي در حال آزمايش RNA پيامرسان براي مسلحكردن سيستم ايمني دربرابر ويروسها يا سرطان هستند، فقط چند شركت كارآزماييهاي باليني كوچكي براي درمانهاي ديگر (مانند استفاده از mRNA براي جايگزينكردن پروتئينهاي ازدسترفته يا معيوب) آغاز كردهاند. در جدول زير، به برخي از اين شركتها اشاره شده است.
بسياري ديگر از داروهاي mRNA بايد ازطريق جريان خون به مكان خاصي از بدن برسند. يك مورد نقص اورنيتين ترانس كارباميلاز (OTC) است كه فقدان آنزيمي موجب تجمع آمونياك در خون ميشود و به تشنج و كما و مرگ ميتواند منجر شود. براي پيشگيري از تجمع آمونياك، داروي mRNA بايد به سلولهاي كبد برسد.
شركت آركتوروس درزمينهي داروهاي mRNA فعاليت ميكند و يكي از اهدافش درمان OTC است. بهگفتهي جوزف پين، رئيس شركت يادشده، اين شركت قصد دارد با تنظيم اندازه و بار الكتريكي نانوذرات ليپيدي مقدار دارويي را به حداكثر برساند كه به كبد ميرسد. شركت آركتوروس مطالعهي ايمني اوليه را درحدود سي داوطلب سالم بهاتمام رسانده است و اين ماه، دوازده فرد مبتلا به نقص مذكور داروي شركت را دريافت كردند. از علل تمركز آركتوروس روي نقص OTC اين بود كه كبد معمولا ذرات را از جريان خون بهدام مياندازد و آنها را جمع ميكند كه نانوذرات درماني را نيز شامل ميشود.
جيمز دهلمن، متخصص مهندسي زيستپزشكي در مؤسسهي فناوري جورجيا، ميگويد رساندن mRNA به بافتهاي ديگر سختتر است. گروههاي پژوهشي مختلفي مشغول دستكاري ساختار نانوذرات ليپيدي يا مزينكردن آنها با مولكولهايي هستند كه آنها را بهسوي ارگان يا سلولهاي خاصي هدايت ميكند. آزمايشگاه دهلمن و شركت گايد تراپيوتيكس (Guide Therapeutics) كه او از بنيانگذارانش است، تكنيكي براي رديابي مسير هزاران نانوذرهي منحصربهفرد ازانديشه متخصصين شيميايي با برچسبگذاري آنها با باركدهاي DNA ايجاد كرده است. بااينحال، او ميگويد كشف ارتباط ميان ساختار نانوذرهي ليپيدي و مقصدش يك دهه طول خواهد كشيد.
دومين تفاوت بزرگ ميان واكسنها و درمانهاي مبتنيبر mRNA آن است كه واكسنها فقط به يك يا چند دُز نياز دارند. وقتي سيستم ايمني براي حمله به تهديد مدانديشه متخصصين يادگيري ديد، پروتئين توليدشده از mRNA تخريب ميشود و به جايگزيني مجدد نياز ندارد.
بهگفتهي دهلمن، داروهاي mRNA كه تاكنون به كارآزماييهاي باليني رسيدهاند، در بيشتر مواقع داروهايي هستند كه اثر دارو بيش از طول عمر دارو است. اين وضعيت براي روشهايي درماني نيز وجود دارد كه از mRNA براي رمزگذاري پروتئينهايي مانند آنزيم Cas9 استفاده ميكند. آنزيم Cas9 ژنوم براي ايجاد ويرايشهاي دائمي برش ميدهد.
اينتليا تراپيوتيكس (Intellia Therapeutics)، شركت فعال درزمينهي ويرايش ژنوم به روش كريسپر، روي درمان مبتنيبر mRNA براي بيماري ارثي آميلوئيدوز ترانستيرتين كار ميكند. اين شركت داروي خود را ماه گذشته به اولين شركتكننده كارآزمايي باليني داد.
وقتي براي تأمين مجدد پروتئين در طول زندگي به تكرار دُزهاي mRNA نياز باشد، عوارض جانبي (احتمالا ناشي از تجمع نانوذرات ليپيدي در بدن يا پاسخ التهابي به RNA خارجي) بزرگتر ميشود. آن باربير، از شركت ترنسليت بيو (Translate Bio)، شركت فعال درزمينهي درمانهاي mRNA ميگويد: «مردم ممكن است يكيدو روز ناراحتي و تب را پس از دريافت واكسن كوويد ۱۹ را بپذيرند؛ اما اينكه اين وضعيت را در تمام طول عمرتان هر سه هفته يك بار يا بيشتر تحمل كنيد، پيشنهاد متفاوتي است.»
شركت ترنسليت بيو و شركتهاي ديگر براي اينكه دُزهاي مكرر دارو قابلتحملتر باشد، مشغول طراحي mRNA هستند كه تاحدممكن براي بدن طبيعي بهانديشه متخصصين برسد و آن را ازطريق نانوذرات زيستتخريبپذير تحويل ميدهند. درمان mRNA شركت ترنسليت بيو براي فيبروز كيستيك اكنون در مرحلهي آزمايشهاي باليني است. بهگزارش اين شركت، يك دُز واحد از اين درمان عارضهي جانبي جدي بههمراه نداشت؛ ولي برخي بيماران دچار تب و درد عضلاني يا سردرد شدند كه كوتاهمدت و مهارشدني بود. گفتني است كارآزمايي ديگري نيز در حال آزمايش دُزهاي متعدد است.
افزايش مقدار پروتئيني كه بدن از يك دُز mRNA ميسازد، موجب كاهش فراواني و اندازهي دُزهاي موردنياز ميشود. ساهاي ميگويد يكي از روشها آن است كه توانايي نانوذرات ليپيدي را در فرار از آن دسته از كيسههاي غشايي افزايش دهيم كه سلول براي گيرانداختن آنها استفاده ميكند. بدينترتيب، مقدار بيشتري از محمولهي mRNA نانوذرات فرصتي براي تعامل با ماشينآلات سلولي براي ساخت پروتئين پيدا ميكند. تيم وي ماه فوريه گزارش كرد كه در آزمايشهاي انجامشده روي سلولها، گنجاندن انواع طبيعي كلسترول در نانوذرات ليپيدي موجب شد آنها بتوانند بهتر فرار كنند.
رقابت براي ساخت واكسن mRNA عليه كوويد ۱۹ اشكالات تحويل و استعمال مكرر درمانهاي mRNA را برطرف نكرده است؛ اما شايد مسير آنها را ازطريق ديگري هموار كرده باشد. موضوعي كه توليدكنندگان واكسن نشان دادهاند، اين است كه توليد ميلياردها نانوذره و رشتهي mRNA در زمان كوتاهي امكانپذير است. تيم ساهاي هنوز در حال كشف بهترين نانوذرات ليپيدي براي همراهي و رساندن mRNA به بخشهاي دورازدسترس بدن است. او رسيدن به چنين كشفي را تحولآفرين ميخواند؛ چراكه اكنون مراحل رسيدن اين درمانها به كلينيك هموار شده است.
هم انديشي ها