طراحي واكسني جديد براي بيماري آلزايمر

پژوهشگران مركز پزشكي دانشگاه تگزاس اخيرا گزارش كردند كه آنها واكسني را طراحي كردهاند كه ميتواند بدن را در حمله به پلاكهاي آميلوئيدي و كلافههاي نوروفيبريلي بيماري آلزايمر قبل از اينكه مغز را مختل كنند، مسلح كند. آنها اميدوارند كه اين واكسن را بهزودي روي انسانها آزمايش كنند. واكسن جديد براي نخستين بار پلاكهاي حاوي آميلوئيد و پروتئين تائو را كه هر دو شاخصيهايي براي تشخيص قطعي بيماري آلزايمر هستند، مورد هدف قرار ميدهد. در اين واكسنها از DNAي پروتئينهاي آلزايمر براي يادگيري سيستم ايمني در جهت مبارزه با اين عناصر و جلوگيري از تجمع آنها در مغز استفاده ميشود. پژوهشگران ميگويند كه اين واكسن جديد آلزايمر كه DNA Aβ42 ناميده ميشود، ميتواند تعداد موارد زوال عقل را به نصف برساند. پژوهشگران نتايج اين مطالعه را در ژورنال Alzheimer’s & Research Therapy منتشر كردند.
واكسن جديد بر خلاف موارد پيشين، از طريق تزريق سطحي در پوست استعمال ميشود. نمونههاي قبلي كه بهصورت تزريق عضلاني در موشها مورد استفاده قرار ميگرفتند، موجب تورم مغز ميشدند. پس از تزريق پوستي واكسن جديد، يك زنجيرهي سهملكولي (تريمر) از بتاآميلوئيد در پوست ساخته شده و بدن با توليد آنتيباديهايي كه مانع از افزايش آميلوئيد و تائو ميشود، به اين ملكولها پاسخ ميدهد. راجر روزنبرگ نويسندهي مقاله ميگويد:
اهميت اين يافتهها اين است كه ايمنيدرماني تريمر DNA Aβ42 دو عامل بيماريزاي بيماري آلزايمر يعني پلاكهاي آميلوئيد و كلافههاي نوروفيبريل را بدون ايجاد پاسخ التهابي سلولهاي T كه خطر بروز التهاب خودايمني را به همراه دارند، مورد هدف قرار ميدهد.
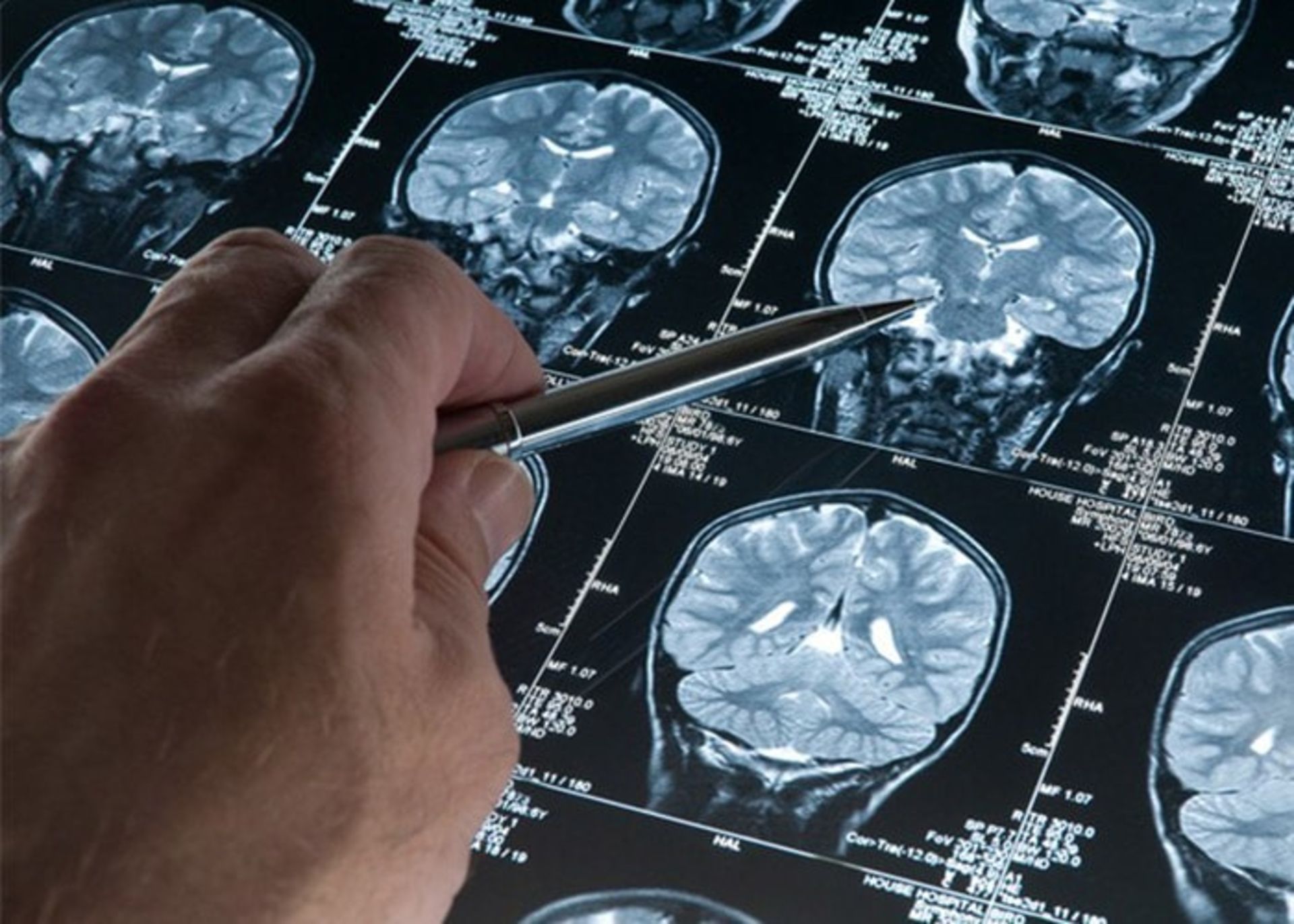
از آنجايي كه در حال حاضر پژوهشگران بهطور دقيق نميدانند كه چه زماني تجمع آميلوئيد و تائو آغاز ميشود، روزنبرگ ميگويد كه پزشكان با انجام اسكنهاي مغزي ميتوانند تعيين كنند كه چه زماني اين واكسن بايد استفاده شود.
اگرچه پژوهش روزنبرگ ارتباطي با مطالعه رادولف تانزي، دانشمند دانشگاه هاروارد كه ژنهاي مرتبط با آغاز آلزايمر را مورد مطالعه قرار داد، ندارد ولي هر دو به يك موضوع اشاره دارند: با كم نگهداشتن سطح آميلوئيد، از بروز آلزايمر اجتناب كنيد.
آزمايشگاه تانزي در بيمارستان عمومي ماساچوست در حال مكانيابي ميكروبيوم مغز است؛ جمعيتي از ميكروارگانيسمها كه برخي مفيد بوده و برخي بيماريزا هستند و درون مغز وجود دارند. پژوهشگران در پروژه ميكروبيوم مغز، بهدنبال يافتن شايعترين ميكروبها در مغز هستند. هدف آنها اين است كه تعيين كنند كدام ميكروبها ميتوانند منجر به بروز بيماري آلزايمر شوند. با استفاده از اين اطلاعات، آنها اميدوارند كه درمانهايي براي پيشگيري و درمان اين بيماري پيدا كنند.
اين كار جداي سيستم كشت سهبعدي سلولهاي عصبي يا مدل بيماري آلزايمر در يك ظرف (ارگانوئيدهاي شبيهسازيشده از مغز انسان) است كه تانزي و دكتر دو توئن كيم با استفاده از ژنهاي آلزايمر ايجاد كردند. اين سيستم اساسا وضعيتي تقليدي از فرايندهاي تشكيل پلاكها و كلافهها در بيماري آلزايمر است. با استفاده از اين سيستم، تانزي دارويي براي بيماري آلزايمر معرفي كرد كه حاوي تنظيمكنندههاي آنزيم گاما سكرتاز و چاپرونهاي فلزي براي كم كردن بتا آميلوئيد و تشكيل كلافههاي نوروفيبريلي در مغز بود.
او گفت اين پژوهش فوقالعاده پيچيده است؛ دانشمندان از سلولهاي بنيادي براي توليد سلولهاي عصبي انسان استفاده كردند. سپس آنها را در ژلي قرار دادند تا مغز انسان را شبيهسازي كنند و توانستند كل فرايند بيماريزايي آلزايمر را در ظروف آزمايشگاهي ايجاد كنند. اين كار به آنها اين امكان را ميداد كه بتوانند حوادث واقعي را كه بهطور معمول طي چند دهه پيش ميآيد، مشاهده كنند: تشكيل پلاكهاي آميلوئيد كه سپس منجر به تشكيل كلافهها و التهاب در مغز ميشوند.
تانزي گفت مدل آلزايمر در يك ظرف مسئلهاي بهقدمت چند دهه را در مورد اينكه آيا پلاكهاي آميلوئيد يا كلافههاي نوروفيبيرلي براي بيماري آلزايمر بايد مورد سرزنش قرار گيرند، حل كرد. ديگر ترديدي وجود ندارد؛ تمام دادهها ميگويند كه اگر شما مقدار آميلوئيد را كم نگه داريد، آلزايمر را متوقف خواهيد كرد. او ميگويد:
ما تا زماني كه علايم آلزايمر قابل مشاهده شوند، آن را مورد درمان قرار نميدهيم و در اين زمان علت آن يعني پلاكهاي آميلوئيدي را درمان ميكنيم. لازم است كه تشكيل پلاكهاي آميلوئيدي را ۱۰ تا ۲۰ سال قبلتر از آنكه علايم در فرد قابل مشاهده شوند، متوقف كنيم. ما اكنون ميتوانيم با استفاده از تصويربرداري از مغز و بيوماركرهايي، احتمال اينكه يك فرد در مراحل بعدي زندگي دچار آلزايمر شود را تعيين كنيم؛ درست مانند كاري كه پزشكان با آزمايش كلسترول براي بيماري قلبي انجام ميدهند. در آينده نزديك، تستهاي خوني براي آلزايمر نيز وجود خواهد داشت.
تانزي اميدوار است كه در آيندهاي نزديك، بههمين ترتيب كه آمريكاييها از دارويي براي پيشگيري از تجمع كلسترول استفاده ميكنند، دارويي نيز براي پايين نگهداشتن سطوح آميلوئيد مغز ارائه شود.
روش ديگر هم استفاده از واكسن روزنبرگ خواهد بود. پژوهشگران در مطالعه خود نوشتند:
ما براي اولين بار با مطالعه روي يك موشهاي مبتلا به آلزايمر گزارش ميكنيم كه ايمنيدرماني با استفاد از DNA Aβ42 فعال در پوست دو عامل بيماريزا را مورد هدف قرار ميدهد: پلاكهاي حاوي آميلوئيد و تائو.
واكسيناسيون DNA كه در آن آنتيژني (پپتيد يا پروتئين) موجود نيست اما DNAي كدكننده اين پپتيد وجود دارد، روش ديگري براي واكسيناسيون است. ژنهاي كدشده توسط DNA در پوست بيان پيدا ميكنند و اين پپتيدها توسط سلولهاي دندريتيك به گرههاي لنفي محلي برده شده و با سلولهاي T و B مواجه ميشوند.
پژوهشگران مركز پزشكي دانشگاه تگزاس نشان دادهاند كه ايمنيدرماني تريمر DNA Aβ42 فرايندي غيرالتهابي بوده و موجب پاسخ ايمني ميشود كه در حذف آميلوئيد از مغز موشهاي ترانسژنيك موثر است. اكنون آنها دريافتهاند كه ايمنيدرماني با تريمر DNA Aβ42 منجر به كاهش پپتيدهاي آميلوئيد و پلاكهاي آميلوئيد ميشود. براي نخستين بار است كه ايمنيدرماني DNA Aβ42 منجر به كاهش قابلتوجهي در پروتئين تائو در معز موش ميشود.
آلزايمر بهعنوان يك بيماري تخريبكنندهي عصب، شايعترين فرم زوال عقل است كه در جمعيت مسن مشاهده ميشود. روزنبرگ و دانشمندان ديگر براي سالها معتقد بودهاند كه ايمنيدرماني با هدف مبارزه با تجمع آميلوئيد در مغز ميتواند درمان ممكني براي آلزايمر باشد و ممكن است بتواند به جلوگيري از پيشرفت بيماري كمك كند. تعدادي از روشهاي ايمنيدرماني كه قبلا انجام شده بودند، بينتيجه بودهاند. يكي از اين موارد، روشي بود كه پژوهشگران متوجه شدند موجب بروز بيماري انسفاليت خودايمني در ۶ درصد از بيماران ميشود.
امروزه بيماري آلزايمر ششمين علت مرگومير در آمريكا است. اين بيماري مغز افراد مبتلا را دچار اشكال ميكند؛ پروتئينهاي آميلوئيد بتا، با افزايش سن در مغز به هم ميچسبند و كلافههايي از پروتئينهاي تائو تشكيل ميشود كه مانع از ارتباطات عصبي ميشوند. درماني براي اين بيماري وجود ندارد و در حال حاضر فقط گزينههاي درماني در جهت كاهش علايم در دسترس هستند. ويژگيهاي پاتوژنيك پلاكهاي آميلوئيدي و كلافههاي نوروفيبريلي علايم تشخيص قطعي بيماري آلزايمر محسوب ميشوند و منشا و توسعهي بيماري بهطور قوي با تجمع آميلوئيد بتا در مغز مرتبط بوده است. حدود ۳۰ سال پيش، فرضيه آبشار آميلوئيد با اين فرض كه رسوب آميلوئيد اولين رويداد منجر به بيماري آلزايمر است، ارائه شد.
واكسن روزنبرگ كه در پوست اعمال ميشود، موجب توليد يك زنجيرهي سه ملكولي از بتاآميلوئيد در سلولهاي پوست ميشود. در اين وضعيت سيستم ايمني فعال ميشود تا آنتيباديهايي براي مبارزه با پروتئين تائو و آميلوئيد بتا توليد كند. پژوهشگران اين واكسن را روي چهار گروه از موشها آزمايش كردهاند. كاهش ۴۰ درصدي در پلاكهاي آميلوئيدي در موشهاي واكسينهشده مشاهده شد و تا ۵۰ درصد از ميزان كلافههاي تائو نيز در مغزشان كم شد.
پژوهشگران گفتهاند كه آنها پاسخ ايمني نامطلوبي در ارتباط با اين واكسن مشاهده نكردند و اين نتايج نشان ميدهد كه با اين واكسن، بدن براي حمله به پلاكهاي آميلوئيد و كلافههاي تائو قبل از اينكه اينها شروع به از كار انداختن مغز كنند، مسلح ميشود.
هم انديشي ها