كشف ويروسهاي غولپيكر داراي ويژگيهاي منحصر به فرد
پژوهشگران با مطالعه ژنهاي موجود در محيطهاي مختلفي مانند بزاق انسان، مدفوع حيوانات، بيمارستانها، خاك و موارد ديگر، صدها ويروس غولپيكر پيدا كردهاند. برخي از اين ويروسها داراي قابليتهايي هستند كه تا پيش از اين تنها در حيات سلولي ديده شده بود.
يك گروه پژوهشي بينالمللي تحت هدايت دانشمنداني از دانشگاه بركلي كاليفرنيا گروههاي كاملا جديدي از فاژهاي غولپيكر را پيدا كردهاند (ويروسهايي كه باكتريها را آلوده ميكنند) و ۳۵۱ توالي ژني را با هم تركيب كردند. پژوهشگران درون اين تواليها، ژنهايي را پيدا كردند كه ويژگيهاي غيرمنتظرهاي را كدگذاري ميكردند ازجمله بخشهايي از دستگاه سلولي را كه دستورالعملهاي DNA را براي ساخت پروتئين خوانده و اجرا ميكند (فرايند ترجمه). باسم الشايب و جيل بانفيلد از دانشگاه بركلي در مصاحبه با ساينسآلرت گفتند:
آنها داراي تعداد غيرمعمولي از اجزاي دستگاه ترجمه هستند كه در يك ويروس معمولي ديده نميشود.
فرايند ترجمه در ساختارهاي مولكولي موسوم به ريبوزمها صورت ميگيرد و پژوهشگران واقعا ژنهايي را پيدا كردند كه برخي از مولفههاي آنها (پروتئينهاي ريبواخبار تخصصيي) را كدگذاري ميكردند. روهان ساچدوا متخصص اكولوژي ميكروبي از دانشگاه بركلي گفت:
بهطور معمول، چيزي كه زنده را از غيرزنده جدا ميكند، داشتن ريبواخبار تخصصي و توانايي ترجمه است. اين يكي از مهمترين ويژگيهايي است كه ويروسها را از باكتريها جدا ميكند. برخي از فاژهاي بزرگ داراي ماشينآلات ترجمه زيادي هستند، بنابراين اين مرزبندي را تا حدودي مبهم ميكنند.
پژوهشگران همچنين تواليهاي كدكنندهي سيستم كريسپر را نيز پيدا كردند. سيستم كريسپر بهعنوان سيستم ايمني كه باكتريها از آن براي مقابلهبا ويروسها استفاده ميكنند، نيز وجود دارد. ويروسهاي تازه كشفشده همه داراي ژنومهايي با طول بيش از ۲۰۰ هزار جفت نوكلئوتيد هستند درحاليكه ميانگين اندازهي ژنوم فاژهاي شناختهشده، بيشتر و درحدود ۵۲ هزار جفت باز است.
برخي از ژنومهاي فاژي كه پژوهشگران شناسايي كردند واقعا غولآسا بودند؛ پژوهشگران يك گروه را «فاژهاي غولآسا» ناميدند و در نامگذاري ۹ گروه جديد ديگر نيز از كلمهي «بزرگ» استفاده كردند. الشايب و بانفيلد گفتند:
ژنوم اين فاژها حداقل ۴ برابر ژنوم يك فاژ معمولي است و بزرگترين آنها ۱۵ برابر حالت معمول بوده و ۷۳۵ هزار جفت باز دارد.
تصور ميشود اين فاژهاي بزرگتر باعث آلودهشدن باكتروئيدها شوند. باكتروئيدها گروهي از باكتريها هستند كه بهطور گسترده در محيط پيراموان ما و از خاك گرفته تا رودههاي ما حضور دارند. ژنوم اين فاژهاي سنگين به اندازهي كافي بزرگ است كه رقيب ژنوم باكتريهاي كوچك شود اما پاندورا ويروسهاي آلودهكنندهي آميب همچنان با ۲/۵ ميليون جفت باز، مقام اول بزرگترين ژنوم ويروسي را دارند. ساچدوا گفت:
فاژهاي بزرگي قبلا شناسايي شدهاند اما آنها يافتههاي پراكندهاي بودند. چيزي كه ما در اين مقاله پيدا كرديم، آن است كه اينها اساسا همه جا هستند. ما آنها را درجايي ميبينيم.
همچون ساير فاژها، اين گروهاز ويروسها، DNA خود را به ميزبان باكتريايي خود تزريق ميكنند و تجهيزات تكثير ژن قرباني را براي ساخت نسخههاي از خودشان به خدمت ميگيرند. پژوهشگران گمان ميكنند كه حين اين اتفاق، فاژهاي غولپيكر همچنين از برخي از ژنهاي اضافي خود براي تغيير مسير مراحل اوليه ترجمه درون باكتري استفاده ميكنند و توليد پروتئين را متناسب با نياز خود منحرف ميكنند. چنين كنترلي از توليد پروتئين در ويروسهاي جانوري ديده شده است.
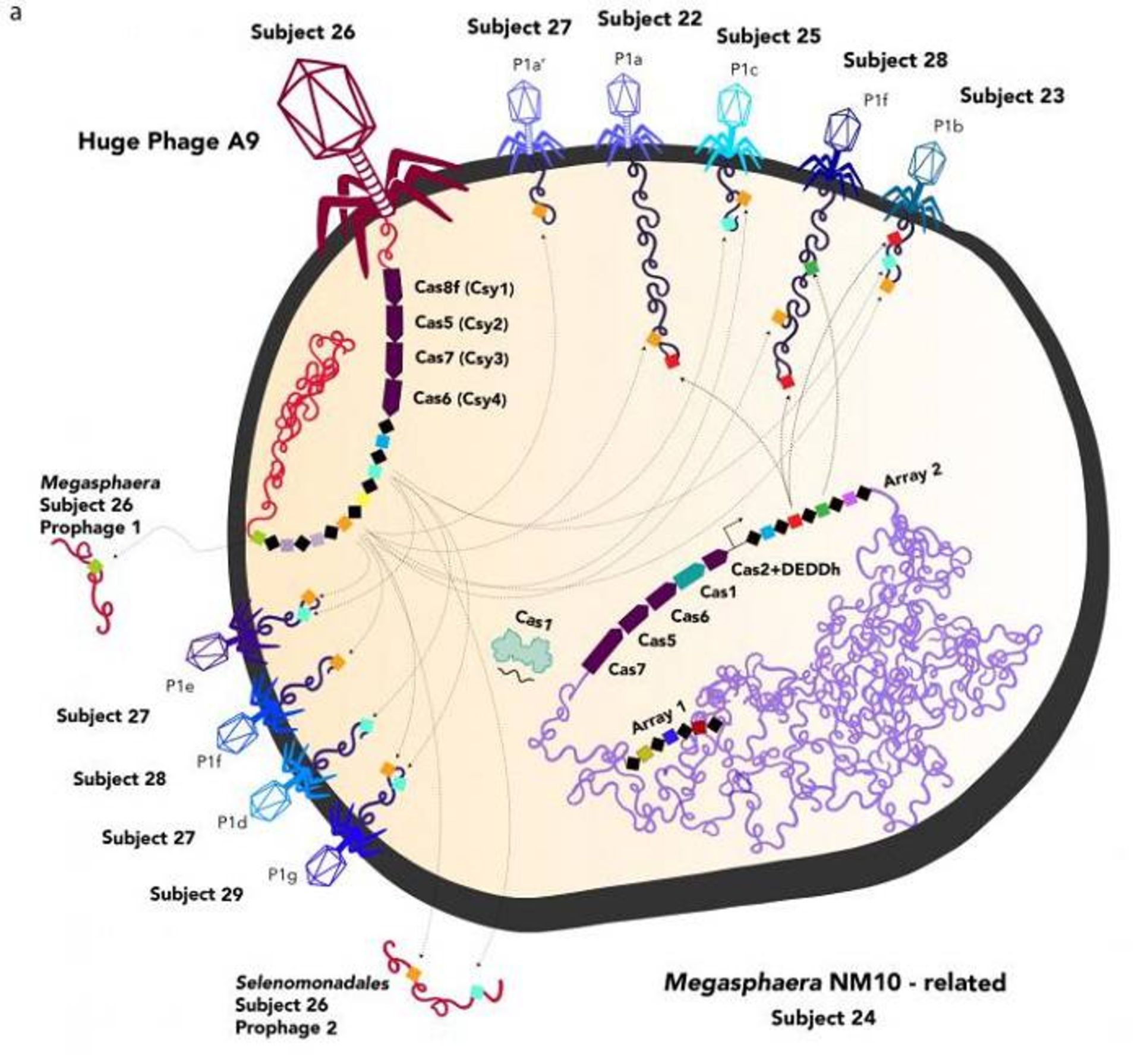
يك فاژ غولپيكر (مورد ۲۶) يك باكتري را آلوده كرده و پاسخ آن دربرابر فاژهاي ديگر را دستكاري ميكند
الشايب توضيح داد كه فاژهاي غولپيكر از سيستم كريسپر خود براي جنگ فاژ دربرابر فاژ استفاده ميكنند و ويروسهاي رقيبي را كه قصد دارند همان باكتري ميزبان را آلوده كنند، بهطور اختصاصي مورد هدف قرار ميدهند. مطالعهاي كه در سال گذشته منتشر شد، نشان داد كه چگونه برخي از فاژها از اين سيستم براي خنثيكردن اقدامات ضدفاژي باكتري ميزبان استفاده ميكنند. بانفيلد گفت:
چيزي كه با نگاه كردن به اين ژنومهاي بزرگ متوجه ميشويم، آن است كه فاژها ژنها و مسيرهاي مختلف زيادي را بهدست آوردهاند؛ برخي از آنها را ميتوانيم پيشبيني كنيم و برخي را نيز نميتوانيم پيشبيني كنيم زيرا درجريان عفونت، فاژ واقعا كنترل عملكرد ميزبان باكتريايي خود را به دست ميگيرد.
هرچه درمورد ارتباطات بين سلامت جسم و روان و ميكروبهايي كه درون بدن و محيط پيرامون زندگي ميكنند، دانش بيشتري كسب ميكنيم، بيشتر متوجه ميشويم كه هرچيزي كه روي اين جوامع باكتريايي اثر بگذارد، ميتواند تاثير عميقي روي ما نيز داشته باشد. الشايب گفت:
فاژها همچنين به انتقال ژنهاي كدكنندهي سموم باكتريايي و مقاومت آنتيبيوتيكي بين باكتريها معروف هستند. از آن جايي كه ما هم باكتريهاي مفيد و هم باكتريهاي مضر را داريم كه روي سطح بدن و نيز داخل بدن ما زندگي ميكنند، درك اينكه چه انواعي از فاژها همراه باكتريها در بدن انسانها و حيوانات وجود دارند و چگونه روي محيطهاي مذكور تاثير ميگذارند، از اهميت زيادي برخوردار است.
پژوهشگران پيشنهاد ميكنند كه سيستمهاي كريسپري كه برخي از اين فاژها دارند، شايد اين قابليت را داشته باشد كه به ما كمك كند تا با تغيير عملكرد باكتريها يا حذف باكتريهاي اشكالساز، ميكروبيوم خود را كنترل كنيم. الشايب و بانفيلد اكنون اميدوارند كه برخي از اين فاژهاي غولآسا را در آزمايشگاه پرورش دهند تا درمورد سيستمهاي كريسپر فاژها دانش بيشتري بهدست آورند و نقشهاي آنها را كشف كرده و ارزش آنها را در ويرايش ژن ارزيابي كنند. كريستوف ويگل، متخصص بيوشيمي كه در اين مطالعه مشاركتي نداشته است، ميگويد مقالهي حاضر از ايدهي درانديشه متخصصينگرفتن ويروسها بهعنوان «ويروسل زنده» حمايت ميكند. بانفيلد توضيح داد:
اين فاژهاي عظيم، شكاف بين «باكتريوفاژهاي غيرزنده» و «باكتريها و آركياها» را پر ميكنند. قطعا استراتژيهاي موفقي براي زندگي وجود دارد كه تركيبي از ويروس معمولي و ارگانيسمهاي زنده معمولي است.
اگرچه مطالعهي حاضر درمورد تنوع زيستي ويروسها نيز دانش زيادي همراه خود دارد، درحالحاضر، مهمترين مباحثهي كه پيش ميآيد، معناي واقعي زنده بودن است.
نتايج اين پژوهش در مجلهي Nature منتشر شده است.
هم انديشي ها